Tài liệu ôn tập Học kì II môn Hóa học Lớp 10 năm học 2019- 2020
Bạn đang xem tài liệu "Tài liệu ôn tập Học kì II môn Hóa học Lớp 10 năm học 2019- 2020", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Tài liệu ôn tập Học kì II môn Hóa học Lớp 10 năm học 2019- 2020
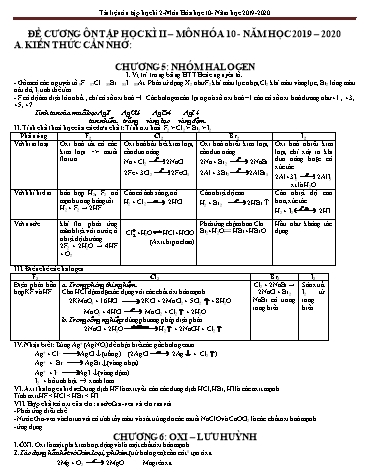
ĐỀ CƯƠNG ÔN TẬP HỌC KÌ II – MÔN HÓA 10 - NĂM HỌC 2019 – 2020 A. KIẾN THỨC CẦN NHỚ: CHƯƠNG 5: NHÓM HALOGEN I. Vị trí trong bảng HTTH các nguyên tố. - Gồm có các nguyên tố 9F 17Cl 35Br 53I 85At. Phân tử dạng X2 như F2 khí màu lục nhạt, Cl2 khí màu vàng lục, Br2 lỏng màu nâu đỏ, I2 tinh thể tím. - F có độ âm điện lớn nhất , chỉ có số oxi hoá –1. Các halogen còn lại ngoài số oxi hoá –1 còn có số oxi hoá dương như +1 , +3 , +5 , +7 Tính tan của muối bạc AgF AgCl¯ AgBr¯ AgI¯ tan nhiều trắng vàng lục vàng đậm II. Tính chất hoá học của các đơn chất: Tính oxi hoá F2 > Cl2 > Br2 > I2 Phản ứng F2 Cl2 Br2 I2 Với kim loại Oxi hoá tất cả các kim loại => muối florua Oxi hoá hầu hết kim loại, cần đun nóng Na + Cl2 2NaCl 2Fe + 3Cl2 2FeCl3 Oxi hoá nhiều kim loại, cần đun nóng 2Na + Br2 2NaBr 2Al + 3Br22AlBr3 Oxi hoá nhiều kim loại, chỉ xảy ra khi đun nóng hoặc có xúc tác 2Al +3I2 2AlI3 xt là H2O Với khí hidro hỗn hợp H2, F2 nổ mạnh trong bóng tối. H2 + F2 → 2HF Cần có ánh sáng, nổ H2 + Cl2 2HCl Cần nhiệt độ cao H2 + Br2 2HBr Cần nhiệt độ cao hơn, xúc tác H2 + I2 2 HI Với nước khí flo phản ứng mãnh liệt với nước, ở nhiệt độ thường 2F2 + 2H2O → 4HF + O2 Cl+H2OHCl+HClO (Axit hipoclorơ) Phản ứng chậm hơn Clo Br2+H2O HBr+ HBrO Hầu như không tác dụng III. Điều chế các halogen F2 Cl2 Br2 I2 Điện phân hỗn hợp KF và HF a. Trong phòng thí nghiệm Cho HCl đậm đặc tác dụng với các chất ôxi hóa mạnh 2KMnO4 + 16HCl 2KCl + 2MnCl2 + 5Cl2 + 8H2O MnO2 + 4HCl MnCl2 + Cl2 + 2H2O b. Trong công nghiệp: dùng phương pháp điện phân 2NaCl + 2H2OH2 + 2NaOH + Cl2 Cl2 + 2NaBr → 2NaCl + Br2 NaBr có trong rong biển Sản xuất I2 từ rong biển IV. Nhận biết: Dùng Ag+ (AgNO3) để nhận biết các gốc halogenua. Ag+ + Cl- AgCl ¯ (trắng) (2AgCl 2Ag + Cl2) Ag+ + Br- AgBr ¯ (vàng nhạt) Ag+ + I- AgI ¯ (vàng đậm) I2 + hồ tinh bột ® xanh lam VI. Axit halogenhidric: Dung dịch HF là axit yếu còn các dung dịch HCl, HBr, HI là các axit mạnh Tính axit HF < HCl < HBr < HI VII. Hợp chất có oxi của clo: nước Gia-ven và clorua vôi - Phản ứng điều chế - Nước Gia-ven và clorua vôi có tính tẩy màu và sát trùng do các muối NaClO và CaOCl2 là các chất oxi hoá mạnh - ứng dụng CHƯƠNG 6: OXI – LƯU HUỲNH I. ÔXI. Oxi là một phi kim hoạt động và là một chất ôxi hóa mạnh 1. Tác dụng hầu hết với kim loại, phi kim (trừ halogen): cần có t0 tạo ôxit 2Mg + O2 2MgO Magiê oxit S + O2 SO2 C + O2 CO2 2. Tác dụng với các hợp chất. CH4 + 2O2 CO2 + 2H2O C2H5OH + 3O2 → 2CO2 + 3H2O 3. Điều chế oxi a. PTN: Nhiệt phân KMnO4 rắn, KClO3 rắn : 2KMnO4 K2MnO2 + MnO2 + O2 b. CN: Chưng cất phân đoạn không khí lỏng hoặc điện phân nước II. ÔZÔN là dạng thù hình của oxi và có tính ôxi hóa mạnh hơn O2 rất nhiều 2Ag + O3 Ag2O + O2 (ở điều kiện thường oxi không có phản ứng) III. LƯU HUỲNH là chất ôxi hóa nhưng yếu hơn O2, ngoài ra S còn đóng vai trò là chất khử khi tác dụng với oxi 1. S là chất oxi hóa khi tác dụng với kim loại và H2 tạo sunfua chứa S2- Tác dụng với nhiều kim loại (có t0,tạo sản phẩm ứng số oxy hoá thấp của kim loại) Fe + S0 FeS-2 sắt II sunfua Hg + S HgS-2 thủy ngân sunfua, phản ứng xảy ra ở t0 thường. Tác dụng với H2: tạo hidro sunfua mùi trứng ung (trứng thối ) H2 + S H2S-2 hidrosunfua 2. S là chất khử khi tác dụng với chất ôxi hóa tạo hợp chất với số oxi hoá dương (+4, +6) Tác dụng với một số phi kim S + O2 SO2 khí sunfurơ, lưu huỳnh điôxit, lưu huỳnh (IV) ôxit. S + 3F2 → SF6 IV. HIDRÔSUNFUA (H2S) là chất khử mạnh 1. Tác dụng với oxi có thể tạo S hoặc SO2 tùy lượng ôxi và cách tiến hành phản ứng. 2H2S + 3O22H2O + 2SO2 (dư ôxi, đốt cháy) 2H2S + O22H2O + 2S 2. Dung dịch H2S có tính axit yếu : Khi tác dụng dung dịch kiềm có thể tạo muối axit hoặc muối trung hoà H2S + NaOH NaHS + H2O H2S + 2NaOH Na2S + 2H2O 3. Điều chế khí H2S: PTN từ phản ứng FeS + 2HCl ® FeCl2 + H2S . Công nghiệp không sản xuất V. LƯU HUỲNH ĐIOXIT công thức hóa học SO2, ngoài ra có các tên gọi khác là lưu huỳnh dioxit hay khí sunfurơ, hoặc anhidrit sunfurơ. 1. Tính chất hoá học: a. SO2 là một oxit axit: tác dụng với nước tạo axit sunfurơ H2SO3 SO2 + NaOH NaHSO3 hoặc SO2 + 2 NaOH Na2SO3 + H2O b. SO2 vừa là chất khử, vừa là chất oxi hoá 2 + Br2 + 2H2O → 2HBr + H24 (SO2đóng vai trò là chất khử) 2 + 2H2S ® 2H2O + 3(SO2đóng vai trò là chất oxi hoá) 2. Điều chế a. Phòng thí nghiệm: Na2SO3 + H2SO4 Na2SO4 + H2O + SO2 b. Công nghiệp: 4FeS2 + 11O2 2Fe2O3 + 8SO2 VI. LƯU HUỲNH (VI) OXIT công thức hóa học SO3, ngoài ra còn tên gọi khác lưu huỳnh tri oxit, anhidrit sunfuric. Là một ôxit axit Tác dụng với H2O tạo axit sunfuric: SO3 + H2O ® H2SO4 + Q Tác dụng với oxit bazơ và bazơ tạo muối sunfat: SO3 + 2 NaOH ® Na2SO4 + H2O VII. AXÍT SUNFURIC H2SO4 ở trạng thái loãng là một axit mạnh, ở trạng thái đặc là một chất ôxi hóa mạnh. 1. Tính chất của axit sunfuric loãng là axít mạnh làm đỏ quì tím, tác dụng kim loại(trước H2) giải phóng H2, tác dụng bazơ, oxit bazơ và nhiều muối. 2. Tính chất của axit sunfuric đặc là một chất ôxihóa mạnh và có tính háo nước a. Tính oxi hoá mạnh: axit sunfuric đặc nóng oxi hoá hầu hết các kim loại (trừ Au và Pt), nhiều phi kim (C,S,P...) và nhiều hợp chất: 2Fe + 6 H2SO4 Fe2(SO4)3+ 3SO2+ 6H2O Cu + 2 H2SO4 CuSO4 + SO2 + 2H2O Lưu ý: Al, Fe, Cr không tác dụng với H2SO4 đặc nguội, vì kim loại bị thụ động hóa. 2H2SO4(đ) + C CO2 + 2SO2 + 2H2O 2H2SO4(đ) + S 3SO2 + 2H2O FeO + H2SO4 (đ) Fe2(SO4)3 + SO2 + 4H2O b. Tính háo nước: hấp thụ nước của một số chất hữu cơ. Ví dụ: nhỏ H2SO4(đ) vào đường saccarozơ C12H22O11 + H2SO4(đ) → 12C + H2SO4.11H2O 2H2SO4(đ) + C CO2 + 2SO2 + 2H2O 3. Điều chế axit sunfuric - Sản xuất SO2 từ FeS2 hoặc S: 4FeS2 + 11O2 2Fe2O 3 + 8SO2 hoặc S + O2 SO2 - Oxi hoá SO2 2SO2 + O2 2SO3 - Hấp thụ SO3 bằng H2SO4: SO3 + H2SO4 H2SO4.nSO3 (ôleum) H2SO4.nSO3 + n H2O ® (n+1) H2SO4 4. Nhận biết ion sunfat: Nhận biết gốc SO42- (sunfat) dùng dung dịch muối bari như BaCl2 hoặc Ba(OH)2. Tạo kết tủa trắng BaSO4 không tan trong axit BaCl2 + Na2SO4 → BaSO4 ¯ + 2NaCl BaCl2 + H2SO4 → BaSO4 ¯ + 2HCl B. PHẦN TRẮC NGHIỆM: CHƯƠNG V :NHÓM HALOGEN. Dung dịch axit nào sau đây không thể chứa trong bình thủy tinh? A. HF. B. HCl. C. HBr. D. HI. Cấu hình electron lớp ngoài cùng chung cho các halogen là A. ns2 np4. B. ns1 np6. C. ns2 np5. D. ns2 np3. Trong các halogen sau: F2, Cl2, Br2, I2. Đơn chất halogen có tính oxi hoá yếu nhất là A. F2. B. I2. C. Br2. D. Cl2. Đặc điểm nào dưới đây là tính chung cho các Halogen? A. Ở điều kiện thường đều là chất khí. B.Vừa có tính oxi hoá vừa có tính khử. C. Có tính oxi hoá mạnh. D. Tác dụng mạnh với nước. Dung dịch nào sau đây dùng để nhận biết hồ tinh bột? A. KI. B. I2. C. KBr. D. Br2. Có các đặc điểm nhận xét về các đơn chất halogen a. Ở điều kiện thường là chất khí. b. Có tính oxi hóa mạnh. c. Vừa có tính oxi hóa vừa có tính khử. d. Tác dụng mạnh với nước. e. Nhận thêm 1e trong phản ứng hóa học. f. Có cấu hình electron lớp ngoài cùng ns2np5. Số đặc điểm chung là A. 2. B. 3. D. 4. C.5. Khi nói về sự biến đổi tính chất vật lí của các đơn chất halogen (từ flo đến iot), tính chất nào không đúng? A. Trạng thái tập hợp: từ thể khí sang thể lỏng và rắn. B. Màu sắc đậm dần: lục nhạt-vàng lục-nâu đỏ-đen tím. C. Nhiệt độ nóng chảy tăng dần. D. Nhiệt độ sôi giảm dần . Điều nào không đúng khi nói về nguyên tố clo? A. Có độ âm điện lớn nhất . B. Tác dụng hầu hết các kim loại tạo muối MCln. C. Tồn tại trong vỏ trái đất với trữ lượng lớn. D. Chất khí dùng làm chất diệt trùng nước sịnh hoạt. Trong phòng thí nghiệm, khí Clo được điều chế bằng cách khử hợp chất nào sau đây? A. MnO2 B. HCl C. KClO3 D. KMnO4 Khi hòa tan clo vào nước ta thu được nước clo có màu vàng nhạt . Khi đó một phần clo tác dụng với nước. Vậy nước clo có chứa những chất gì ? A. HCl, HClO B. Cl2, HCl, HClO. C. H2O, Cl2, HCl, HClO. D. Cl2, HCl, H2O. Clo tác dụng được với tất cả các chất ở dãy nào sau đây? A. H2, H2O, NaBr, Na. B. H2, Na, O2, Cu. C. H2, Cu, H2O, O2. D. H2O, Fe, N2, Al. Trong dãy axit HF- HCl- HBr- HI. Theo chiều từ trái sang phải tính chất axit biến đổi như sau? A. Tăng. B. Giảm. C. Không thay đổi. D. Vừa tăng vừa giảm. Trong các dãy chất dưới đây, dãy nào gồm các chất đều tác dụng được với dung dịch HCl? A. Fe2O3, KMnO4, Cu. B. Fe, CuO, Ba(OH)2. C. CaCO3, H2SO4, Mg(OH)2. D. AgNO3(dd), MgCO3, BaSO4. Phản ứng nào sau đây chúng tỏ HCl có tính khử ? A. 4HCl + MnO2 → MnCl2 + Cl2 + 2H2O. B. 2HCl + Mg(OH)2 → MgCl2 + 2H2O. C. 2HCl + CuO → CuCl2 + H2O. D. 2HCl + Zn → ZnCl2 + H2. Chất nào sau đây không thể dùng làm khô chất khí Hidro clorua? A. P2O5. B. NaOH rắn. C. dd H2SO4 đặc D. CaCl2 khan. Kim loại nào sau đây, khi tác dụng với clo và axit HCl đều tạo ra cùng một loại muối? A. Fe. B. Cu. C. Mg. D. Ag. Muối clorua có rất nhiều ứng dụng, muối NaCl có thể sát trùng, bảo quản thực phẩm. Hoa quả tươi, rau sống được ngâm trong dd NaCl từ 10-15 phút trước khi ăn. Khả năng diệt khuẩn của dung dịch NaCl là do A. dung dịch NaCl có thể tạo ra Cl- có tính khử. B. vi khuẩn bị mất nước do thẩm thấu. C. dung dịch NaCl độc. D. một lí do khác. Nước gia-ven là hỗn hợp của các chất nào sau đây? A. HCl, HClO, H2O. B. NaCl, NaClO, H2O. C. NaCl, NaClO3, H2O. D. NaCl, NaClO4, H2O. Nước gia-ven có tính oxi hóa cao, nên có nhiều ứng dụng, ứng dụng nào sau không phải của nước gia-ven? A. Tẩy trắng quần áo, vải, sợi, giấy. B. Là chất khử trùng, khử mùi. C.Tẩy uế chuồng trại chăn nuôi, nhà vệ sinh. D. Ngâm rau sống, hoa quả tươi khử trùng trước khi ăn. Cho các phát biểu sau: a) CaCO3 tan trong dung dịch HCl. b) Hỗn hợp gồm CuO, Al, Fe tan hết trong dd HCl dư. c) Trong phản ứng Cl2 + 2NaOH → NaCl + NaClO + H2O, clo vừa là chất khử vừa là chất oxi hóa. d F2, Cl2, Br2 oxi hóa được H2O. e) Dung dịch HF không thể chứa trong bình thủy tinh. f) Khi ta thêm dần dần nước clo vào dung dịch KI có chứa sẵn một ít hồ tinh bột thì dung dịch có màu xanh đặc trưng Số phát biểu đúng là A. 3 B.4 C.5 D.6 Nếu cho 1 mol mỗi chất: CaOCl2, KMnO4, K2Cr2O7, MnO2 lần lượt phản ứng với lượng dư dung dịch HCl đặc, chất tạo ra lượng khí Cl2 nhiều nhất là A. KMnO4. B. MnO2 C. CaOCl2. D. K2Cr2O7. Phát biểu nào sau đây đúng? A. Iot có bán kính nguyên tử lớn hơn brom. B. Dung dịch NaF phản ứng với dung dịch AgNO3 sinh ra AgF kết tủa. C. Flo có tính oxi hoá yếu hơn clo. D. Axit HBr có tính axit yếu hơn axit HCl. Phát biểu nào sau đây không đúng? A. Trong các hợp chất, ngoài số oxi hoá -1, flo và clo còn có các số oxi hoá +1, +3, +5, +7. B. Muối AgI không tan trong nước, muối AgF tan trong nước. C. Flo có tính oxi hóa mạnh hơn clo. D. Dung dịch HF hòa tan được SiO2. Bao nhiêu gam Clo đủ để tác dụng với kim loại Nhôm tạo thành 26,7g muối nhôm clorua? A. 23,1g. B. 21,3g. C. 12,3g. D. 13,2g. Khi clo hóa 30g hỗn hợp bột đồng và sắt cần 14 lít khí Cl2 (đktc). Thành phần % khối lượng của Cu trong hỗn hợp ban đầu? A. 46,6%. B. 53,3%. C. 55,6% . D. 44,5%. Thu được bao nhiêu mol Cl2 khi cho 0,2 mol KClO3 tác dụng với dung dịch HCl đặc dư? A. 0,3mol. B. 0,4 mol. C. 0,5mol. D. 0,6mol. Cho 20g hỗn hợp bột Mg, Zn và Fe tác dụng với dd HCl dư thấy có 1g khí bay ra. Hỏi có bao nhiêu gam muối Clorua tạo ra trong dung dịch? A. 40,5g. B. 45,5g. C. 55,5g. D. 60,5g. Dùng 150ml dd HCl để kết tủa hoàn toàn 200g dd AgNO3 8,5%. Nồng độ của dd HCl là A. 0,67M. B. 0,1 M. C. 1M. D. 0,2M. Cho 22g hỗn hợp Fe và Al tác dụng với dd HCl dư thu được 17,92 lít khí (đktc). Thành phần % khối lượng mỗi chất trong hỗn hợp ban đầu là A. 50,9% và 49,1%. B. 25,45% và 74,54%. C. 76,36% và 23,64%. D. 33,45% và 66,55% Cho 0,54g kim loại R (hóa trị không đổi) tác dụng với dd HCl dư thu được 672cm3 khí H2 (đktc). Xác định R. A. Zn. B. Ca. C. Al. D. Mg. Cho 1,2 g kim loại M tác dụng với dd HCl dư tạo thành 4,75g muối clorua. Xác định tên kim loại. A. Zn. B. Ca. C. Al. D. Mg. Cho 1,44g hỗn hợp (Mg, Fe, Cu) tác dụng vừa đủ với clo thu được 3,925g hỗn hợp muối X, hòa tan X vào nước rồi cho dd NaOH đến dư vào, lọc thu được m gam kết tủa. Giá trị m là A. 2,63g. B. 2,36g. C. 3,26g. D. 3,39g. Hòa tan hoàn toàn 30,6g hỗn hợp gồm Na2CO3 và CaCO3 trong dd HCl vừa đủ thu được 6,72 lít khí (đktc) và dung dịch muối X. Cô cạn X thu được m gam muối khan. Giá trị của m là A. 40,5g. B. 45,5g. C. 39,3g. D. 33,9g. CHƯƠNG VI: OXI- LƯU HUỲNH Tính chất hoá học đặc trưng của oxi là A. chất oxi hoá mạnh. B. chất khử mạnh. C. vừa có tính oxi hoá, vừa có tính khử. D. không có tính oxi hóa. Ứng dụng nào sau đây không phải của ozon? A. Tẩy trắng tinh bột, dầu ăn. B. Chữa sâu răng, bảo vệ hoa quả. C. Khử trùng nước uống, khử mùi. D. Điều chế oxi trong PTN. Có các kết luận sau: a. Cấu hình electron của nguyên tử oxi là 1s22s22p4. b. Khí oxi không phản ứng được với Cl2. c. Ozon có thể được dùng để tẩy trắng tinh bột, chữa sâu răng, sát trùng nước sinh hoạt. d. Sắt khi tác dụng với HCl và H2SO4 loãng đều thu được muối sắt (II). e. Sắt khi tác dụng với Cl2 và H2SO4 đặc nóng đều thu được muối sắt (III). f. Có thể phân biệt khí SO2 và CO2 bằng dung dịch nước brom. Số kết luận đúng là A. 6. B. 3. C. 5. D. 4. Trong các câu sau, câu nào sai: A. oxi tan nhiều trong nước. B. Oxi nặng hơn không khí. C. oxi chiếm 1/5 thể tích không khí. D. Oxi là chất khi không màu, không mùi, không vị. Phản ứng điều chế oxi trong phòng thí nghiệm là A. 2KMnO4 K2MnO4 + MnO2 + O2. B. 2KClO3 2KCl + 3O2. C. KNO3 KNO2 + O2. D. 2H2O (điện phân) " 2H2 + O2 Có các kết luận sau a. S là chất rắn vừa có tính khử, vừa có tính oxi hóa. b. S có thể phản ứng được với Al, O2, F2, H2, H2SO4 đặc. c. Lưu huỳnh là chất rắn có màu vàng, tác dụng với thủy ngân ngay nhiệt độ thường. d. S không tan trong nước, tan trong một số dung môi hữu cơ. e. S có 5 electron ở lớp ngoài cùng. f. S tà phương (Sα) và S đơn tà (Sp) là hai dạng thù hình. Số phát biểu đúng là A. 6. B. 3. C. 5. D. 4. Trong phản ứng: 3S + 6KOH 2K2S + K2SO3 + 3H2O. Lưu huỳnh đóng vai trò là A. không là chất oxi hóa cũng không là chất khử. B. chất khử. C. là chất oxi hóa nhưng đồng thời cũng là chất khử. D. chất oxi hóa. Tính chất hóa học đặc trưng của H2S là A. vừa oxi hóa vừa khử. B. tính axit yếu, tính khử mạnh. C. tính oxi hóa. D. tính khử. Có các kết luận sau: a. Sục khí H2S vào dung dịch CuSO4 thấy xuất hiện kết tủa đen. b. Dung dịch H2S để lâu ngày trong không khí có màu vàng. c. H2S là chất khí, không màu, không mùi. d. Trong tự nhiên H2S có trong khí núi lửa và xác động vật thối rửa. e. Trong phòng thí nghiêm H2S được điều chế bằng cách cho FeS tác dụng với d ung dịch HCl. f. Khi dẫn H2S vào dung dịch NaOH (tỉ lệ mol 1:1) thu được muối NaHS. Số kết luận đúng là A. 6. B. 3. C. 5. D. 4. Phản ứng nào sau đây không thể xảy ra ? A. Na2S + 2HCl H2S + 2NaCl. B. CuS + 2HCl CuCl2 + H2S. C. FeS + 2HCl FeCl2 + H2S. D. CuSO4 + H2S CuS + H2SO4. Cho các phản ứng sau: (1) SO2 + H2O H2SO3 ;(2) SO2 + NaOH → NaHSO3 ; (3) SO2 + CaO →CaSO3; (4) SO2 + 2H2S→ 3S +2H2O. Có bao nhiêu phản ứng mà SO2 là một oxit axit? A. 1. B. 2. C. 3. D. 4. Có các kết luận sau: a. Để pha loãng dung dịch H2SO4 đặc người ta đổ từ từ nước vào axit. b. H2SO4 đặc chỉ có tính oxi hoá mạnh, không có tính axit c. H2SO4 đặc rất háo nước. d. Kim loại Al, Fe,Cr không tác dụng với H2SO4 đặc, nguội. e. Hấp thụ SO3 vào H2SO4 đặc 98% được oleum. f. H2SO4 dùng để sản xuất thuốc trừ sâu, phân bón, chất giặt rửa tổng hợp. Số kết luận đúng: A. 6. B. 3. C. 5. D. 4. Cho các chất : Cu, NaOH, Al, C, ZnO, NaCl, HI, FeO, Fe2O3. Axit Sunfuric đặc, nóng phản ứng với bao nhiêu chất sinh ra khí SO2? A. 7. B. 4. C. 6. D. 5. Trong số những tính chất sau, tính chất nào không là tính chất của axit H2SO4 đặc nguội? A. Tan trong nước, tỏa nhiệt. B. Làm hóa than vải, giấy, đường. C. Hòa tan được kim loại Al và Fe. D. Háo nước. Cho các chất khí sau đây: Cl2, SO2, CO2, SO3, H2S. Chất làm mất màu dung dịch brom là: A. CO2, SO2, B. SO3, SO2, C. SO2 , H2S D. Cl2, H2S Dãy đơn chất nào sau đây vừa có tính oxi hóa vừa có tính khử? A. Br2, O2, Ca. B. S, Cl2, Br2. C. Na, F2, S. D. Cl2, O3, S. Cho sơ đồ phản ứng:H2SO4đặc,nóng + Fe ® Fe2(SO4)3 + SO2 + H2O. Số phân tử H2SO4 bị khử và số phân tử H2SO4 tham gia tạo muối trong PTHH của phản ứng trên là: A. 6 và 3. B. 3 và 6. C. 6 và 6. D. 3 và 3. Hấp thụ 2,24 lít SO2 (đktc) vào 250 ml dung dịch NaOH 1M thu được dung dịch X. Chất tan có trong dung dịch X: A. Na2SO3 và NaOH dư. B. Na2SO3. C. NaHSO3 và Na2SO3. D. NaHSO3. Oxi hóa hoàn toàn 3,06 gam hỗn hợp gồm Al và Mg bằng oxi thu được 5,46g hỗn hợp oxit. Thể tích oxi cần dùng ở đktc là A. 1,68. B. 2,68. C. 1,792. D. 1,344. Cho 20g hỗn hợp X gồm Fe, Cu phản ứng hoàn toàn với H2SO4 loãng dư, sau phản ứng thu được 12g chất rắn không tan. Phần trăm về khối lượng của Fe trong X là A.60% . B. 72% . C. 40% . D. 64%. Hòa tan hết 6,9g kim loại R trong dung dịch H2SO4 vừa đủ thu được 3,36 lít khí H2 (đktc). Kim loại R là A. Na B. Mg C. K D. Zn Cho 11,2 g kim loại tác dụng hết với H2SO4 đặc, nóng thu được 6,72 lít khí SO2 (đktc). Tên kim loại là A. Cu B. Fe C. Zn D. Al. Hòa tan 1,2g Mg trong axit sunfuric đặc nóng, thu được 0,28 lít (đktc) một sản phẩm khử X của lưu huỳnh. Công thức của X là A. SO2 B. H2S C. S D. H2SO3 Hoà tan hoàn toàn 3,22g hỗn hợp X gồm Fe, Mg, Zn bằng một lượng vừa đủ H2SO4 loãng thấy thoát 1,344 lít H2 ở đktc và dung dịch chứa m gam muối. Giá trị của m là A. 10,27g B.8.98 C.7,25g D. 9,52g Cho 7,8g hỗn hợp Mg và Al tác dụng với dung dịch H2SO4 loãng dư, thu được 8,96 lít khí (đktc). Phần trăm về khối lượng của Mg trong hỗn hợp là A. 30,77% B. 69,23% C. 61,53% D. 38,47% Cho 11gam hỗn hợp X gồm Al và Fe tác dụng với một lượng dư axit H2SO4 (đặc, nóng) , sau phản ứng thu được 10,08 lít khí SO2 (đktc,sản phẩm khử duy nhất). Phần trăm về khối lượng của Al trong hỗn hợp là A. 33,7% B. 49,1% C. 50,9% D. 38,4% Có thể dùng chất nào sau đây để nhận biết các dung dịch mất nhãn riêng biệt: H2SO4, BaCl2, Ba(OH)2, Na2SO4 A. Quỳ tím. B. AgNO3. C. Na2CO3. D. A và C. clorua vôi kali clorua nước javen B. TỰ LUẬN: Hoàn thành sơ đồ chuyển hóa sau: a/ Mangan đi oxit khí clo hydro clorua natri clorua clo b) FeS2 → SO2 → SO3 → H2SO4 → SO2→ S → FeS → H2S→ SO2 → H2SO4 →CuSO4 → BaSO4 c) H2S → S → SO2 → SO3 → H2SO4 → FeSO4 → Fe(OH)2 Trong phòng thí nghiệm có các hóa chất: NaCl, MnO2, H2SO4 đặc, NaOH, Ca(OH)2, Fe, S. và Viết các phương trình hóa học điều chế nước Javen, Clorua vôi, hidrosunfua, sắt (II) clorua, sắt (III) clorua. Cho 17,4g MnO2 tác dụng hết với dung dịch HCl lấy dư. Toàn bộ khí clo sinh ra được hấp thụ hết vào 145,8g dung dịch NaOH 20% ( ở nhiệt độ thường ) tạo ra dung dịch A. Hỏi dung dịch A có chứa những chất tan nào ? Tính nồng độ phần trăm của từng chất tan đó . Cho m gam hỗn hợp gồm (Mg, Fe) tác dụng vừa đủ với 0,896 lit clo. Cũng m gam hỗn hợp trên tác dụng với dd HCl dư thu được 0,672 lít khí (các khí đo ở đktc). a) Viết các phương trình phản ứng xảy ra. b) Tính m? Nung m gam hỗn hợp gồm (Zn và S) trong bình kín không có không khí được hỗn hợp rắn X, hòa tan X trong 200 ml dd HCl aM thu được 0,448 lít hỗn hợp khí Y có tỉ khối so với hidro là 9. a)Tính m. b) Tính a, biết dd HCl dùng dư 20% so với lượng phản ứng? Hòa tan 12 gam hỗn hợp Fe và Cu trong dung dịch H2SO4 loãng dư, thu được 2,24 lít khí (đktc). Chất rắn còn lại được đem hòa tan trong dung dịch H2SO4 đặc nóng dư thu được khí SO2. a) Tính % khối lượng mỗi kim loại trong hỗn hợp đầu. b) Dẫn toàn bộ lượng SO2 ở trên vào 550 ml dd NaOH 1M. Tính khối lượng các chất tạo ra trong dd thu được? Một hỗn hợp gồm bột Fe và Cu. Chia hỗn hợp làm 2 phần bằng nhau: Phần 1: Cho tác dụng với dd H2SO4 loãng (dư) thu được 4,48 lít khí (ở đktc) Phần 2: Cho tác dụng với dd H2SO4 đặc nóng (dư) thu được 8,96 lít khí SO2 (đktc). Tính khối lượng và % khối lượng mỗi kim loại trong hỗn hợp ban đầu? Câu 68: Nung 1,12g Fe với 0,32g S trong bình kín không có không khí được hỗn hợp rắn X, hòa tan X trong 200 ml dd HCl aM thu được hỗn hợp khí Y và dd Z. a) Tính tỉ khối của hỗn hợp Y so với hidro? b) Để trung hòa dd HCl còn dư trong Z cần 300ml dd NaOH 0,1M. Tính a? Câu 69:Trình bày cách nhận biết các dung dịch sau. Viết phương trình hóa học a) NaCl, Na2SO4, NaNO3, H2SO4 b) HCl, NaOH, Na2SO4, Ba(OH)2, H2SO4 Câu 70:Nhận biết các chất khí: O2, H2S, SO2, HCl .Viết phương trình hóa học
File đính kèm:
 tai_lieu_on_tap_hoc_ki_ii_mon_hoa_hoc_lop_10_nam_hoc_2019_20.doc
tai_lieu_on_tap_hoc_ki_ii_mon_hoa_hoc_lop_10_nam_hoc_2019_20.doc

