Đề thi chọn HSG Thành phố môn Hóa học Lớp 12 Sở GD&ĐT TP Đà Nẵng (Có đáp án)
Bạn đang xem tài liệu "Đề thi chọn HSG Thành phố môn Hóa học Lớp 12 Sở GD&ĐT TP Đà Nẵng (Có đáp án)", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Đề thi chọn HSG Thành phố môn Hóa học Lớp 12 Sở GD&ĐT TP Đà Nẵng (Có đáp án)
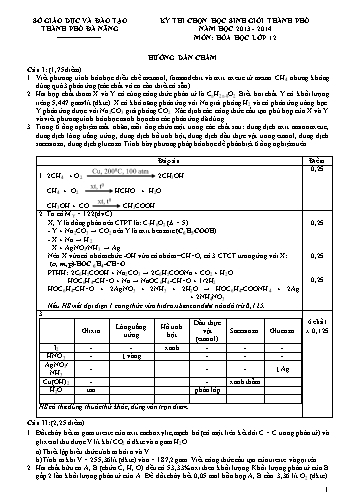
SỞ GIÁO DỤC VÀ ĐÀO TẠO THÀNH PHỐ ĐÀ NẴNG KỲ THI CHỌN HỌC SINH GIỎI THÀNH PHỐ NĂM HỌC 2013 - 2014 MễN: HểA HỌC LỚP 12 HƯỚNG DẪN CHẤM Cõu I: (1,75 điểm) Viết phương trỡnh húa học điều chế metanol, fomandehit và axit axetic từ metan CH4 nhưng khụng dựng quỏ 3 phản ứng (cỏc chất vụ cơ cần thiết cú sẵn). Hai hợp chất thơm X và Y cú cựng cụng thức phõn tử là CnH2n-8O2. Biết hơi chất Y cú khối lượng riờng 5,447 gam/lớt (đktc). X cú khả năng phản ứng với Na giải phúng H2 và cú phản ứng trỏng bạc. Y phản ứng được với Na2CO3 giải phúng CO2. Xỏc định cỏc cụng thức cấu tạo phự hợp của X và Y và viết phương trỡnh húa học minh họa cho cỏc phản ứng đó dựng. Trong 6 ống nghiệm mất nhón, mỗi ống chứa một trong cỏc chất sau: dung dịch axit aminoaxetic, dung dịch lũng trắng trứng, dung dịch hồ tinh bột, dung dịch dầu thực vật trong etanol, dung dịch saccarozơ, dung dịch glucozơ. Trỡnh bày phương phỏp húa học để phõn biệt 6 ống nghiệm trờn. Đỏp ỏn Điểm 2CH4 + O2 2CH3OH CH4 + O2 HCHO + H2O CH3OH + CO CH3COOH 0,25 Ta cú MY = 122 (đvC) X, Y là đồng phõn nờn CTPT là: C7H6O2 (D = 5) - Y + Na2CO3 → CO2 nờn Y là axit benzoic (C6H5COOH) - X + Na → H2 X + AgNO3/NH3 → Ag Nờn X vừa cú nhúm chức -OH vừa cú nhúm –CH=O, cú 3 CTCT tương ứng với X: (o, m, p)-HOC6H4-CH=O PTHH: 2C6H5COOH + Na2CO3 → 2C6H5COONa + CO2 + H2O HOC6H4-CH=O + Na → NaOC6H4-CH=O + 1/2H2 HOC6H4-CH=O + 2AgNO3 + 2NH3 + 2H2O → HOC6H4-COONH4 + 2Ag + 2NH4NO3 Nếu HS viết đại diện 1 cụng thức vừa hiđroxibenzanđehit nào đú trừ 0,125. 0,25 0,25 0,25 Glixin Lũng trắng trứng Hồ tinh bột Dầu thực vật (etanol) Saccarozơ Glucozơ I2 - - xanh - - - HNO3 - ↓ vàng - - - AgNO3/NH3 - - - ↓ Ag Cu(OH)2 - - xanh thẫm H2O tan phõn lớp HS cú thể dựng thuốc thử khỏc, đỳng vẫn trọn điểm. 6 chất x 0,125 Cõu II: (2,25 điểm) Đốt chỏy hết m gam trieste của axit cacboxylic, mạch hở (cú một liờn kết đụi C = C trong phõn tử) và glixerol thu được V lớt khớ CO2 ở đktc và a gam H2O. a) Thiết lập biểu thức tớnh m bởi a và V. b) Tớnh m khi V = 255,36 lớt (đktc) và a = 187,2 gam. Viết cụng thức cấu tạo của trieste và gọi tờn. Hai chất hữu cơ A, B (chứa C, H, O) đều cú 53,33% oxi theo khối lượng. Khối lượng phõn tử của B gấp 2 lần khối lượng phõn tử của A. Để đốt chỏy hết 0,05 mol hỗn hợp A, B cần 3,36 lớt O2 (đktc). Mặt khỏc, lấy 0,05 mol hỗn hợp trờn tỏc dụng với lượng dư dung dịch NaOH thỡ thu được 4,15 gam muối. Biết cỏc phản ứng xảy ra hoàn toàn. Tỡm cụng thức cấu tạo của A và B. Từ metan và cỏc chất vụ cơ cần thiết, viết sơ đồ điều chế chất B. Đỏp ỏn Điểm a. Gọi cụng thức của trieste: CnH2n-10O6 (n12) Áp dụng bảo toàn nguyờn tố oxi, ta cú: = (mol) (gam) Áp dụng bảo toàn khối lượng, ta cú: (gam) b. V = 255,36 lit (đktc) và a = 187,2 gam m = 176,8 gam (đvC) CTCT: C17H33COO)3C3H5: triolein 0,25 0,25 0,25 0,25 a). Gọi cụng thức A, B: CxHyOz (x, y, z nguyờn dương) Với z = 1 ị x = 1, y = 2 là phự hợp. ị CT A, B lần lượt: (CH2O)n và (CH2O)m (m = 2n) Gọi CTPTTB: 0,05 0,05 ị 0,05= 0,15 ị = 3 ị CTPT A: C2H4O2 (M = 60): 0,025 mol B: C4H8O4 (M = 120): 0,025 mol Cú 2 TH: + TH1: A là CH3COOH CH3COOH + NaOH → CH3COONa + H2O RCOOR’ + NaOH → RCOONa + R’OH mr = 4,15 gam Û 0,025(82 + R + 67) = 4,15 ị R = 17 (loại) + TH2: A là HCOOCH3 HCOOCH3 + NaOH → HCOONa + CH3OH RCOOR’ + NaOH → RCOONa + R’OH mr = 4,15 gam Û 0,025(68 + R + 67) = 4,15 ị R = 31 (-CH2OH); R’ = 45 (-CH2CH2OH) Vậy A là HCOOCH3; B là: HOCH2COOCH2CH2OH 0,25 0,25 0,25 0,25 b. (tỉ lệ 1:1) 0,25 Cõu III: (1,5 điểm) X là một α-aminoaxit no, chứa 1 nhúm -COOH và 1 nhúm -NH2. Từ m gam X điều chế được m1 gam đipeptit. Từ 2m gam X điều chế được m2 gam tripeptit. Đốt chỏy m1 gam đipeptit thu được 16,2 gam nước. Đốt chỏy m2 gam tripeptit thu được 30,6 gam H2O. a) Xỏc định giỏ trị của m. b) Thủy phõn hỗn hợp gồm m1 gam đipeptit và m2 gam tripeptit trong 500 ml dung dịch hỗn hợp gồm KOH 1,2M và NaOH 0,8M thu được dung dịch Y. Tớnh khối lượng chất rắn khan thu được khi cụ cạn dung dịch Y. Biết cỏc phản ứng đều xảy ra hoàn toàn. Đỏp ỏn Điểm CT của aminoaxit no, đơn chức, hở X: CnH2n+1O2N (n) : a mol Từ m gam X → m1 gam đipeptit: C2nH4nO3N2 : a/2 mol Từ 2m gam X → m2 gam tripeptit: C3nH6n-1O4N3: 2a/3 mol C2nH4nO3N2 + O2 → 2nCO2 + 2nH2O a/2 mol an mol C3nH6n-1O4N3 + O2 → 3nCO2 + H2O 2a/3 mol mol Theo đề: Vậy m = 89.0,3 = 26,7 (gam) 0,25 0,25 0,25 0,25 nKOH = 0,6 mol; nNaOH = 0,4 mol m1 = 160. 0,15 = 24 gam m2 = 231. 0,2 = 46,2 gam nờn peptit bị thủy phõn hết, kiềm dư. Peptit + kiềm → rắn + H2O Áp dụng ĐLBTKL, ta cú: mrắn = 24 + 46,2 + 0,6.56 + 0,4.40 – 0,35.18 = 113,5 gam 0,25 0,25 Cõu IV: (1,5 điểm) Cho 9,16 gam hỗn hợp A gồm bột kim loại Zn, Fe, Cu vào cốc đựng 170 ml dung dịch CuSO4 1M. Sau khi phản ứng hoàn toàn, thu được dung dịch B và chất rắn C. Nung kết tủa C trong khụng khớ ở nhiệt độ cao tới khối lượng khụng đổi, được 12 gam chất rắn. Chia dung dịch B làm 2 phần bằng nhau: - Thờm NaOH dư vào phần 1, lọc kết tủa, nung trong khụng khớ đến khối lượng khụng đổi, được 5,2 gam chất rắn D. - Điện phõn phần 2 với điện cực trơ trong 10 phỳt với cường độ dũng điện 10 ampe. Tớnh khối lượng mỗi kim loại trong hỗn hợp A. Tớnh khối lượng cỏc chất thoỏt ra ở bề mặt cỏc điện cực. Tớnh thể tớch dung dịch HNO3 1M tối thiểu để hũa tan hết hỗn hợp A tạo sản phẩm khử duy nhất là NO. Đỏp ỏn Điểm Gọi x, y, z lần lượt là số mol của Zn, Fe, Cu cú trong 9,16 gam hỗn hợp A. Zn + CuSO4 → ZnSO4 + Cu Fe + CuSO4 → FeSO4 + Cu Ta cú: = 0,17 và nờn x + y + z < = 0,163 suy ra x + y < 0,17 nờn Zn, Fe tan hết, CuSO4 dư. Chất rắn C là Cu (x+ y + z) mol; dung dịch B chứa ZnSO4, FeSO4 y mol và CuSO4 dư [0,17-(x+y)] mol. Ta cú hệ phương trỡnh: mA= 65x + 56y + 64z = 9,16 nCuO= x + y + z = 12/80 = 0,15 mD= = 5,2 gam Giải ra được: x = 0,04; y = 0,06; z = 0,05. Vậy khối lượng từng kim loại trong hỗn hợp A là: mZn= 2,60 gam, mFe= 3,36 gam, mCu =3,20 gam. HS dựng cỏch khỏc, cỏch tớnh điểm: 3 khối lượng x 0,25. 0,25 0,25 0,25 Dung dịch đem điện phõn gồm 0,02 mol ZnSO4; 0,03 mol FeSO4; 0,035 mol CuSO4. Khi điện phõn, muối CuSO4 bị điện phõn trước. Áp dụng định luật luật Faraday, để CuSO4 bị điện phõn hết cần t = 675 s > 10 phỳt. Nờn chỉ cú CuSO4 bị điện phõn CuSO4 + H2O Cu +1/2 O2 + H2SO4 mCu (ở catot) = 1,99 gam; (ở anot) = 0,4975 gam. 0,25 0,125x2 Cỏc quỏ trỡnh oxi húa- khử: Zn → Zn2+ + 2e Fe → Fe2+ + 2e Cu → Cu2+ + 2e NO3- + 3e + 4H+ → NO + 2H2O (0,04.2 + 0,06.2 + 0,05.2). 4/3 = 0,4 lớt 0,25 Cõu V: (1,5 điểm) Hoàn thành phương trỡnh húa học của cỏc phản ứng sau: K2Cr2O7 + ? + H2O → Cr(OH)3 + S + NH3 + KOH b) K2Cr2O7 + Na2SO3 + H2SO4 → ? + Na2SO4 + K2SO4 + H2O c) K2Cr2O7 + (NH4)2S + ? + H2O → K3[Cr(OH)6] + S + ? Hóy cho biết vai trũ của pH đối với sự tạo thành cỏc sản phẩm chứa crom. Cho m gam hỗn hợp X gồm Ca, CaC2 và Al4C3 (số mol Ca nhỏ hơn số mol của Al4C3) vào nước dư thu được dung dịch A, a gam kết tủa B và 8,96 lớt (đktc) hỗn hợp khớ C cú tỉ khối so với H2 là 8,35. Lọc bỏ kết tủa. Đốt chỏy hoàn toàn hỗn hợp khớ C rồi dẫn sản phẩm chỏy vào dung dịch A thu được thờm a gam kết tủa nữa. Tớnh m. Đỏp ỏn Điểm Phương trỡnh húa học: K2Cr2O7 + 3(NH4)2S + H2O → 2Cr(OH)3 + 3S + 6NH3 + 2KOH K2Cr2O7 + Na2SO3 + H2SO4 → Cr2(SO4)3 + Na2SO4 + K2SO4 + H2O K2Cr2O7 + 3(NH4)2S + 4KOH + H2O →2 K3[Cr(OH)6] + 3S + 6NH3 pH cú ảnh hưởng đến dạng hợp chất của Cr3+, cụ thể: - Mụi trường trung tớnh thỡ Cr3+ ở dạng hiđroxit Cr(OH)3. - Mụi trường axit thỡ Cr3+ ở dạng muối Cr3+, trỏnh thủy phõn. - Mụi trường kiềm thỡ Cr3+ ở dạng phức oxo [Cr(OH)6]3-, cú nhiều OH-. 0,5 0,25 Ca + 2H2O đ Ca2+ + 2OH + H2 x 2x x CaC2 + 2H2O đ Ca2+ + 2OH + C2H2 y 2y y Al4C3 + 12H2O đ 4Al(OH)3 + 3CH4 z 4z 3z Al(OH)3 + OH đ Al(OH) 2x + 2y 2x + 2y 2x + 2y Al(OH) + CO2 đ Al(OH)3 + HCO 2x + 2y 2y + 3z 2x + 2y (x <z) Kết tủa đầu : 4z – (2x + 2y) Kết tủa sau: 2x + 2y Từ giả thiết => 4z – (2x + 2y) = 2x + 2y x + y – z = 0 (1) x + y + 3z = 0,4 (2) mhh khớ = 0,4.8,35.2 = 6,68 => 2x + 26y + 48z = 6,68 (3) Giải hệ phương trỡnh 3 ẩn (1), (2), (3) => x = 0,03; y = 0,07; z = 0,1 m = 0,03.40 + 0,07.64 + 0,1.144 = 20,28 gam. Pt: 0,25 0,25 0,25 Cõu VI: (1,5 điểm) Viết phương trỡnh húa học của phản ứng xảy ra khi cho dung dịch FeCl3 lần lượt tỏc dụng với dung dịch KI, dung dịch AgNO3, dung dịch Na2CO3 và dung dịch KMnO4/H2SO4. Hũa tan hết 18,68 gam hỗn hợp A gồm Fe, Cu trong dung dịch HNO3 loóng thỡ thu được dung dịch B và 5,376 lớt khớ NO (đktc) là sản phẩm khử duy nhất. Trong dung dịch A khối lượng muối sắt nhiều hơn khối lượng muối đồng là 14,44 gam. Tớnh thành phần % khối lượng 2 kim loại trong hỗn hợp A. Đỏp ỏn Điểm Cỏc phương trỡnh húa học xảy ra 2FeCl3 + 2KI → 2FeCl2 + 2KCl + I2 FeCl3 + 3AgNO3 → Fe(NO3)3 + 3AgCl Hoặc FeCl2 + 2AgNO3 → Fe(NO3)2 + 2AgCl 2FeCl3 + 3Na2CO3 + 3H2O → 2Fe(OH)3 + 6NaCl + 3CO2 10FeCl3 + 6KMnO4 + 24H2SO4 →5Fe2(SO4)3 + 3K2SO4 + 6MnSO4 + 15Cl2 + 24H2O 0,75 Vỡ giả thiết khụng cho HNO3 dư nờn cú thể tạo cả sắt (II) và sắt (III) Ta cú cỏc quỏ trỡnh oxi húa và khử Fe → Fe2+ + 2e + 3e → a mol a mol 2a mol 0,72 mol 0,24 mol Fe → Fe3+ + 3e b mol b mol 3b mol Cu → Cu2+ + 2e c mol c mol 2c mol Số mol NO: 5,376:22,4 = 0,24 mol ị số mol e cho = số mol e nhận = 3 ì 0,24= 0,72 mol Ta cú hệ phương trỡnh 56a + 56b + 64c = 18,68 2a + 3b + 2c = 0,72 180a + 242b – 188c = 14,44 ị a = 0,095; b = 0,09; c = 0,13 mol ị % mFe = = 58,46 %; % mCu = 100% - 58,46% = 41,54% 0,25 0,25 0,25 -------------HẾT ------------
File đính kèm:
 de_thi_chon_hsg_thanh_pho_mon_hoa_hoc_lop_12_so_gddt_tp_da_n.doc
de_thi_chon_hsg_thanh_pho_mon_hoa_hoc_lop_12_so_gddt_tp_da_n.doc

