Bài giảng Hóa học Lớp 10 - Bài 23: Hiđro clorua, axit clohiđric, muối clorua - Trường THPT Quang Trung
Bạn đang xem tài liệu "Bài giảng Hóa học Lớp 10 - Bài 23: Hiđro clorua, axit clohiđric, muối clorua - Trường THPT Quang Trung", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Bài giảng Hóa học Lớp 10 - Bài 23: Hiđro clorua, axit clohiđric, muối clorua - Trường THPT Quang Trung
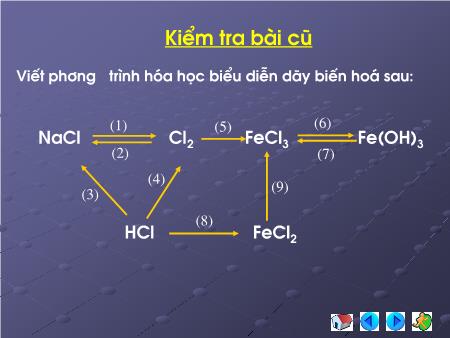
Viết phương trình hóa học biểu diễn dãy biến hoá sau : NaCl Cl 2 FeCl 3 Fe(OH) 3 HCl FeCl 2 Kiểm tra bài cũ (1) (5) (8) (6) (2) (3) (7) (4) (9) Hiđro clorua Cấu tạo phân tử Tính chất II. Axit clohiđric Tính chất vật lí Tính chất hóa học Điều chế III. Muối clorua và nhận biết ion clorua Muối clorua nhận biết ion clorua Hiđro clorua-axit clohiđric-Muối clorua I. Hiđro Clorua 1. Cấu tạo phân tử ( xem mô phỏng ) 2. Tính chất Là khí không màu Nặng hơn không khí ( 1,26 lần) Hít phải nhiều viêm đường hô hấp Tan nhiều trong H 2 O (1V H 2 O hoà tan 500V khí HCl) dd axit HCl II. Axit Clo hiđric : HCl Tính chất vật lý Tính chất hoá học Điều chế 1.Tính chất vật lý Là chất lỏng không màu Tan nhiều trong nước Nồng độ bão hoà khoảng 37% Bốc khói trong không khí ẩm . Vì sao dd HCl đặc bốc khói trong không khí ẩm? 2. Tính chất hoá học: Liên kết cộng hoá trị phân cực H Cl +1 -1 +2e 2H +1 H 2 0 -2e 2Cl -1 Cl 2 0 Ion H + Ion Cl - Tính axit Tính oxi hoá Tính khử Pư trao đổi 2. Tính chất hoá học : Tính chất của axit e) Axit HCl tác dụng muối muối + axit b) Axit HCl tác dụng kim loại đ ứng trước hiđro muối + H 2 VD: 2HCl + Fe = FeCl 2 + H 2 d) Axit HCl tác dụng baz ơ muối + nước c) Axit HCl tác dụng oxit baz ơ muối + nước VD: 2HCl + MgO = MgCl 2 + H 2 O VD: 2HCl + Ba(OH) 2 = BaCl 2 + 2H 2 O VD: 2HCl + CaCO 3 = CaCl 2 + CO 2 + H 2 O HCl + AgNO 3 = AgCl + HNO 3 Trắng a) Axit HCl đ ổi màu chất chỉ thị : Quỳ tím đ ỏ Axit clohiđric Là một axit mạnh Thể hiện tính khử và tính oxi hoá HC l Ngành y tế Phân bón NaCl, KCl, NH 4 Cl CN thực phẩm Đánh gỉ kim loại sơn, mạ, tráng men Cao su cloropren, hiđroclo Chất dẻo P.V.C Muối clorua BaCl 2 , ZnCl 2 , AlCl 3 , CaCl 2 3.Điều chế a) Phòng thí nghiệm : Phương pháp sunfat NaCl + H 2 SO 4 đ → NaHSO 4 + HCl 2NaCl + H 2 SO 4 đ → Na 2 SO 4 + 2HCl b) Trong công nghiệp: ** Phương pháp tổng hợp Cl 2 + H 2 → 2HCl ** Phương pháp sunfat Bài tập 1 ( sử dụng phiếu học tập số 1) Viết 5 phương trình hóa học khác nhau đ iều chế FeCl 2 Đáp án: Fe + 2HCl → FeCl 2 + H 2 FeO + 2HCl → FeCl 2 + H 2 O Fe(OH) 2 + 2HCl → FeCl 2 + 2H 2 O FeCO 3 + 2HCl → FeCl 2 + CO 2 + H 2 O FeSO 4 + BaCl 2 → FeCl 2 + BaSO 4 Bài tập 2 Chỉ dùng kim loại nào dưới đây để phân biệt các dung dịch không màu , đ ựng trong các lọ riêng biệt , mất nhãn : Na 2 CO 3 , HCl , Ba(NO 3 ) 2 ? A. Cu B. Fe C. Ag D. Na Đáp án: Fe Fe + 2HCl = FeCl 2 + H 2 2HCl + Na 2 CO 3 = 2NaCl + CO 2 + H 2 O Còn lại Ba(NO 3 ) 2 Bài tập 3 ( sử dụng Phiếu học tập số 2) Hoàn thành phương trình phản ứng , đ iền các chất vào ch ữ cái : A, B, C, D, E, F MnO 2 + ? A + B + C A + KOH F + G + C A + Cu D D + KOH E xanh + F E + HCl D + C t 0 t 0 t 0 Đáp án: MnO 2 + 4HCl → Cl 2 + MnCl 2 + 2H 2 O (A) (B) (C) 3Cl 2 + 6KOH → 5KCl + KClO 3 + 3H 2 O (A) (F) (G) (C) Cl 2 + Cu → CuCl 2 (A) (D) CuCl 2 + 2KOH → Cu(OH) 2 xanh + 2KCl (D) (E) (F) Cu(OH) 2 + 2HCl → CuCl 2 + 2H 2 O (E) (D) (C) t 0 t 0 Bài tập về nh à: 1. Viết phương trình biểu diễn dãy biến hoá sau đây: Mg MgCl 2 Mg(OH) 2 MgO MgSO 4 MgCl 2 Mg(NO 3 ) 2 (1) (4) (6) (2) (3) (5)
File đính kèm:
 bai_giang_hoa_hoc_lop_10_bai_23_hidro_clorua_axit_clohidric.ppt
bai_giang_hoa_hoc_lop_10_bai_23_hidro_clorua_axit_clohidric.ppt

